A isomeria é um fenômeno químico que acontece quando dois compostos são formados das mesmas moléculas, mas suas fórmulas estruturais diferentes. Quando isso ocorre, são chamados de isômeros. O próprio nome já dá algumas dicas sobre o que representa, sendo iso = igual e meros = partes, ou seja, isômeros são partes iguais.
Tipos de isomeria
Dependendo da forma com que cada estrutura molecular é escrita, são classificadas como isomeria plana ou isomeria espacial. Dentro de cada uma delas, há várias possibilidades de isômeros, os quais foram descritos e exemplificados, abaixo:
Isomeria plana
Os isômeros planos são aqueles em que as fórmulas estruturais estão alinhadas. Eles são classificados da seguinte maneira:
Isomeria de cadeia
A isomeria de cadeia é aquela em que o número de átomos de carbono é diferente para cada composto, no entanto, os demais elementos se distribuem em quantidades e formas iguais.
Exemplo
F.M. C4H10 (metilpropano) e F.M. C3H6 (ciclopropano)
Isomeria de função
Os isômeros de função são aqueles em que os compostos possuem funções químicas diferentes, mas conta com a mesma fórmula molecular.
Exemplo
Tanto a cetona como o aldeído têm a mesma fórmula (CnH2n+2O). Entretanto, eles se diferem pela forma de distribuição:
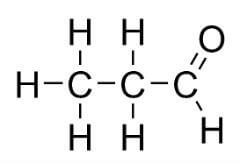
Fórmula da cetona
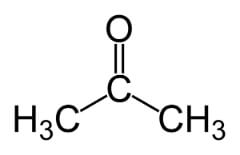
Fórmula do aldeído
Isomeria de posição
A isomeria de posição, como já diz o nome, é aquela em que a cadeia carbônica é a mesma, mas está em posições diferentes ou em um grupo funcional, radical ou de instauração diferentes.
Exemplo
Como mostra na imagem, tanto a fórmula do 2-metil-pentano, como o do 3-metil-pentano são apresentados em posições diferentes na cadeira de ramificação:
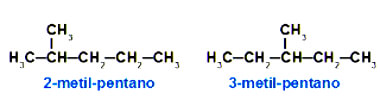
Isomeria de compensação
Também chamada de metameria, esse tipo de isômero ocorre quando os compostos possuem a mesma função química, mas são diferenciados pela posição de cada átomo na cadeia.
Exemplo
É o que ocorre com a estrutura molecular da etil-propilamina e da metil-butilamina. Ambas contam com a mesma fórmula química: C5H13N . No entanto, como pode-se perceber na imagem, abaixo, os elementos N (nitrogênio) e H (hidrogênio) se encontram em heteroátomos diferentes:
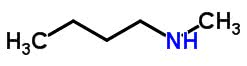
Metil butilamina
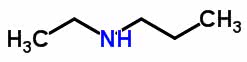
Etil propilamina
Tautomeria ou Isomeria dinâmica
A isomeria dinâmica é determinada pelas fórmulas químicas que, ao mudar um elemento de posição, transformam o composto em outro.
Exemplo
Se mudar a posição do oxigênio na estrutura molecular do etanal (C2H4O), cria-se o etanol, o qual continua tendo a mesma fórmula, mas é escrito de uma maneira diferente. Esse fenômeno pode ser observado na imagem, a seguir:
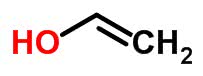
Etanol
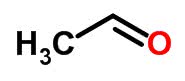
Etanal
Isomeria espacial
Os isômeros espaciais são as fórmulas em que as moléculas de compostos são iguais, mas distribuem-se de forma diferente, o que faz com que os elementos sejam diferentes. São considerados isômeros espaciais:
Isomeria geométrico ou cis-trans
Isomeria cis-trans são as cadeias abertas em que os carbonos se ligam de forma diferente. É justamente isso que faz com que uma mesma fórmula seja classificada como cis ou trans.
Usa-se a determinação cis para as ligações que se encontram do mesmo lado da cadeia. É o caso da fórmula molecular do cis-dicloroeteno (C2H2Cl2):
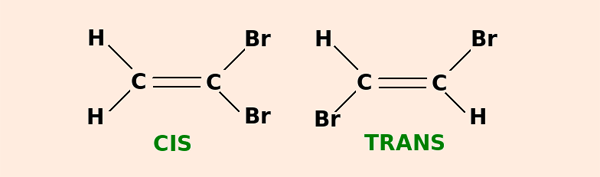
Já o nome trans determina os ligantes que se encontram de lados opostos da cadeia. É por isso que a mesma fórmula do cis-dicloroeteno (C2H2Cl) também pode transformar-se no trans-dicloroeteno.
Isomeria óptica
A isomeria ótica é aquela em que a luz incidente em dois compostos químicos é emitida de forma diferente. Em outras palavras, são as substâncias exatamente iguais, mas que se comportam de modo diferente, quando expostas à luz – seja por conta do índice de refração naquele meio ou pelas propriedades diferenciadas daquele químico.
Em uma ligação covalente, os elétrons são compartilhados entre os átomos envolvidos na ligação. Saiba diferenciar uma ligação Polar e Apolar
👉 Continue Lendo.. Clique aqui